| Публикации: | АСУТП | Теория и технология | Научные работы | Главная |
Металлургия и обработка металлов (выпуск 5)
Материалы научно-технической конференции молодых ученых физико-металлургического факультета
Донецк: ДонНТУ. 2002. С.
Продувке стали аргоном посвящено много работ, в которых предложены уравнения и математические модели позволяющие рассчитать только изменение концентрации водорода. Но, интерес представляет изменение концентрации и других газообразующих элементов в металле (кислород, углерод, азот, сера), состава и расхода отходящих газов.
Рассчитать эти величины можно на детерминированной динамической математической модели. Вывод основных уравнений изменения состава металла и отходящих газов сделан на основе достижения термодинамического равновесия в системе газовый
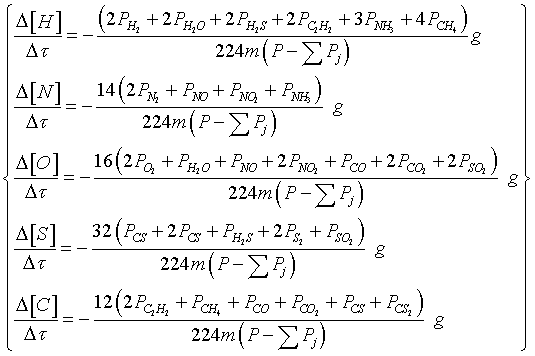
где m – масса стали, т; [Н], [N], [О], [S], [С] – концентрация элемента в стали, %; Р – внешнее давление, атм; 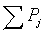 – сумма парциальных давлений всех газов, кроме РAr, атм;
– сумма парциальных давлений всех газов, кроме РAr, атм; 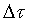 – шаг времени продувки, мин; g – расход аргона, м3/мин.
– шаг времени продувки, мин; g – расход аргона, м3/мин.
Приняты допущения: аргон чистый, в данный момент времени температура и состав стали одинаковые в любой точке объёма, шлаковая фаза на процесс дегазации не влияет, поглощение газов из внешней среды не происходит, газы в пузырьке идеальные, давление в пузырьке равно внешнему (гидростатическое давление металла не учитывалось).
Чтобы уменьшить число неизвестных до пяти, уравнения преобразованы с привлечением зависимостей для констант равновесия реакций дегазации и образования
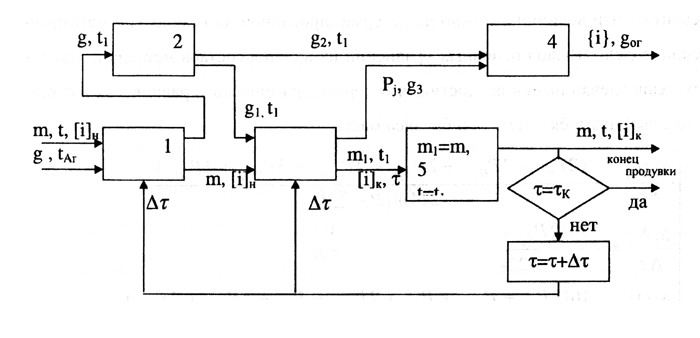
1 – теплообменник; 2 – делитель; 3 – реактор; 4 – смеситель; 5,6 – блоки переприсваивания и условия
Рисунок 1 – Информационная схема процесса.
Входами модели являются масса, температура и химический состав стали (m, t, [i]н); расход и температура аргона (g, 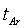 ); шаг и конечное время продувки (
); шаг и конечное время продувки (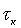 ,
, 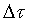 ). В теплообменнике (1) рассчитывается температура металла при охлаждении аргоном. В делителе (2) поток аргона (g) условно разделяется на два (g1 и g2). С потоком g1 коэффициент достижения термодинамического равновесия пузырек аргона – металл равен 1, а с потоком g2 – равен нулю. В реакторе (3) решается система дифференциальных уравнений численным методом
). В теплообменнике (1) рассчитывается температура металла при охлаждении аргоном. В делителе (2) поток аргона (g) условно разделяется на два (g1 и g2). С потоком g1 коэффициент достижения термодинамического равновесия пузырек аргона – металл равен 1, а с потоком g2 – равен нулю. В реакторе (3) решается система дифференциальных уравнений численным методом 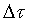 состав стали ([i]к), уменьшенная масса стали (m1), парциальные давления всех газов (Pj) и их расход (g33). В смесителе (4) рассчитывается состав {i} и расход (gог) отходящего газа. В блоке (5) входным величинам присваиваются конечные значения, полученные на предыдущем шаге.
состав стали ([i]к), уменьшенная масса стали (m1), парциальные давления всех газов (Pj) и их расход (g33). В смесителе (4) рассчитывается состав {i} и расход (gог) отходящего газа. В блоке (5) входным величинам присваиваются конечные значения, полученные на предыдущем шаге.
Модель настраивали изменением величины коэффициента в делителе (2), сравнивая расчётные результаты с лабораторными экспериментами [Изв. вуз. Черная металлургия. – 1961, №2. – с.
Результаты сравнения представлены в таблице 1. Наилучшая адекватность модели получена при значении коэффициента достижения равновесия 0.295.
Таблица 1 – Изменение состава стали при продувке
Время, мин |
Изменение состава стали по ходу продувки, % |
|||||
[Н] |
[N] |
[0] |
[S] |
[С] |
||
Эксперимент |
Расчёт по модели | |||||
О |
0.00120 |
0.00120 |
0.0160 |
0.00100 |
0.004 |
0.90 |
5 |
0.00049 |
0.00052 |
0.0081 |
0.00099 |
0.004 |
0.90 |
10 |
0.00035 |
0.00035 |
0.0055 |
0.00099 |
0.004 |
0.89 |
Из табл. 1 следует, что при продувке аргоном уменьшается концентрация растворенных [Н] и [N], а содержание [S], [О], [С] практически не изменяется. Расход отходящих газов (gог) уменьшается по ходу продувки и составил: на 1 мин – 1.705, а на 5 мин – 0.699 м3/мин. Коэффициент использования аргона процесса дегазации для данных экспериментальной продувки оценен равным 0.295.
© А.А. Филипишин, В.Г. Скрябин, 2002
| Вверх |